La crisis sanitaria y social derivada de la pandemia de COVID-19, causada por el coronavirus SARS-CoV-2, han popularizado conceptos como los tests PCR o las pruebas rápidas de detección de la enfermedad. Sin embargo, persisten equívocos y desconocimiento entre el público general que contribuyen en ocasiones a incrementar el desasosiego que produce la actual situación. Desde la Sociedad Española de Medicina de Laboratorio (SEQCML), se quiere contribuir a aclarar algunas cuestiones en torno a las pruebas que se realizan y responder a algunas de las cuestiones que se plantean los ciudadanos, tales como por qué no se están realizando más pruebas, por qué no se pueden realizar más rápido o cuál es la fiabilidad de los tests rápidos.
Las autoridades sanitarias han situado al laboratorio clínico en el centro de la lucha contra la enfermedad, dado que una de las principales recomendaciones de la Organización Mundial de la Salud (OMS) es realizar un adecuado cribado de la población para detectar el alcance real de la infección. El Gobierno español se ha propuesto como próximo objetivo detectar y aislar a los casos asintomáticos, lo cual requiere de la realización de un gran número de pruebas de detección de la enfermedad. Para ponderar correctamente el trabajo del laboratorio en esta lucha, la SEQCML ha elaborado esta nota que incluye las principales claves a tener en cuenta.
Análisis PCR
En primer lugar cabe destacar que un análisis PCR es muy distinto a una prueba rápida. El nombre PCR es el acrónimo inglés de “reacción en cadena de la polimerasa”, una técnica de biología molecular que reproduce in vitro (es decir, en condiciones de laboratorio) el proceso natural de replicación del material genético que todos los seres vivos (animales, vegetales, bacterias, virus…) llevamos a cabo para copiar nuestro material genético y poder, así, reproducirnos y crecer.
“La PCR se lleva a cabo en un equipo automatizado llamado termociclador, pero hasta que la muestra que queremos analizar llega a ese aparato, debe pasar por una serie de procesos. En primer lugar, debemos asegurarnos de que la muestra es adecuada para realizar la técnica, que se ha recogido en el medio de conservación adecuado y que viene correctamente identificada con los datos del paciente al que pertenece. A continuación, es necesario llevar a cabo un proceso de inactivación, para que en caso de que el virus esté presente en la muestra, no contamine nuestros equipos ni tampoco haya riesgos para las personas que trabajan en el laboratorio”, explica la Dra. Imma Caballé, presidenta de la SEQCML.
Una vez inactivada, el siguiente paso consiste en separar el material genético del resto de sustancias y moléculas que están presentes en la muestra y pueden interferir con la PCR. “A este paso lo denominamos extracción de ácidos nucleicos”, detalla la Dra. Caballé, quien precisa que la extracción de ácidos nucleicos puede hacerse de modo manual, pero habitualmente en los laboratorios clínicos se trabaja con máquinas que permiten realizar el proceso en varias muestras a la vez (normalmente entre 12 y 96). En algunos centros se cuenta con equipos robotizados que son capaces de realizar los pasos de extracción de ácidos nucleicos y PCR de forma automática y consecutiva, con poco manejo manual de reactivos y muestras.
Por último, se preparan los reactivos que se debe mezclar con el material genético extraído para que la PCR pueda llevarse a cabo dentro del termociclador. Todo este proceso puede alargarse durante un tiempo, esto depende del equipamiento de los laboratorios y el nivel de automatización disponible. En nuestro país, al igual que en otros, debido a la elevada demanda derivada de esta situación, el proceso se ha venido demorando más de un día, aunque en condiciones óptimas es posible obtener el resultado para 94 muestras en un plazo de unas 2 horas por equipo.
El trabajo del laboratorio clínico en la realización de las pruebas PCR
Los laboratorios de Análisis Clínicos y Microbiología Clínica son los encargados de recibir y analizar las muestras de los pacientes para poder determinar si el virus está presente en las mismas. Los facultativos especialistas en Microbiología son los responsables de decidir cuál es el diseño de PCR más adecuado para detectar cada tipo de patógeno y de interpretar los resultados obtenidos para poder informar a los clínicos. “Estos profesionales son licenciados o graduados en Farmacia, Biología, Bioquímica, Medicina o Química que, tras superar un examen FIR, BIR, MIR o QIR, se forman durante 4 años de residencia en un hospital para poder ejercer como facultativos”, puntualiza la presidenta de la SEQCML.
El manejo de la muestra corre a cargo de los técnicos de laboratorio, personal indispensable que tiene formación en el manejo de muestras biológicas, así como de los fundamentos y la propia realización manual de las técnicas de biología molecular, como la PCR. Todas las Comunidades Autónomas cuentan con laboratorios clínicos hospitalarios y otros centros de diagnóstico. Muchos de ellos tienen la infraestructura necesaria para poder llevar a cabo técnicas de biología molecular como la PCR. En el resto de los casos, se suele asignar un hospital de referencia al que las muestras son trasladadas para poder ser analizadas por otro equipo de microbiólogos.
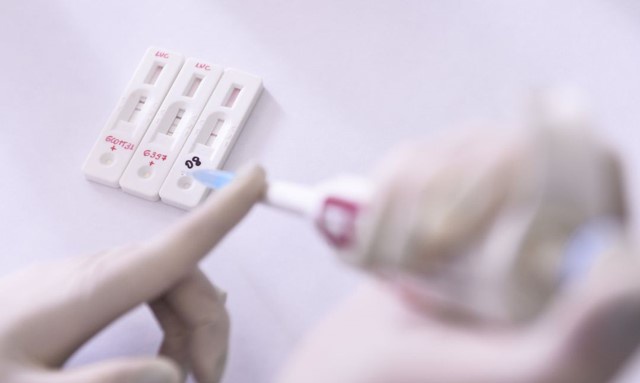
Pruebas rápidas para detectar el SARS-CoV-2
Las pruebas rápidas son un conjunto de técnicas de laboratorio que, como su nombre indica, permiten obtener un resultado en poco tiempo, normalmente menos de 30 minutos. En el caso del SARS-CoV-2, se comercializan pruebas rápidas de dos tipos: de detección de antígeno y de detección de anticuerpos. Los antígenos son moléculas, habitualmente proteínas de microorganismos patógenos, que provocan que el cuerpo humano desarrolle una respuesta inmune. Esta, entre otros mecanismos de defensa, implica la producción anticuerpos específicos para combatir cada microorganismo en cuestión. Las pruebas rápidas se basan en esta relación antígeno-anticuerpo para saber si una persona tiene o ha tenido una infección.
“Las pruebas basadas en la detección de antígeno tienen un anticuerpo al que se unen las proteínas del virus presente en las muestras de las vías respiratorias. Funcionan de forma similar a un test de embarazo. Son pruebas dirigidas a detectar la infección en los primeros 7 días de desarrollo de síntomas, al igual que la PCR en una muestra nasofaríngea, pero son más fáciles de realizar, más baratas y más rápidas. El gran inconveniente es que su sensibilidad, comparada con la PCR, es baja; es decir, un porcentaje de personas que están infectadas, tienen una detección de antígeno negativa”, señala la Dra. Ana Blanco, del servicio de Microbiología molecular de Catlab.
“Por el contrario, en pacientes con más de 7 días de sintomatología, podemos detectar en la sangre anticuerpos frente al virus. En este caso, el test tiene un antígeno al que se unen los anticuerpos generando una banda de color. Por su funcionamiento, cada test utilizado tiene un rendimiento óptimo en un espacio de tiempo concreto y por lo tanto, es importante saber cuánto tiempo hace que el paciente tiene síntomas, para poder elegir la mejor técnica diagnóstica en cada momento”, añade la Dra. Blanco.
Fiabilidad de los tests rápidos
La fiabilidad de una prueba depende de la sensibilidad (capacidad de detectar positivos) y especificidad (capacidad de discriminar negativos, cuando lo son realmente). La PCR es una técnica con gran sensibilidad y especificidad en condiciones óptimas, pero hay que tener en cuenta que, según el tiempo que haya pasado desde que comenzaron los síntomas, el virus puede dejar de ser detectable mediante PCR en muestras obtenidas de la nasofaringe.
Si se compara la prueba PCR con una técnica rápida basada en la detección de proteínas del virus (antígenos) la PCR tiene una sensibilidad muy superior, porque es capaz de detectar cantidades de virus mucho más bajas. Si comparamos la PCR con una técnica rápida de detección de anticuerpos, la respuesta a cuál es más fiable sería “depende”, según precisa la Dra. Blanco. “En función de los días que el paciente lleve enfermo puede que ya no sea posible detectar el virus mediante PCR pero que sí sea posible detectar anticuerpos (es decir, detectar la respuesta inmune que el cuerpo ha generado frente al virus). Hay que tener en cuenta que, en esta situación, se pueden estar detectando infecciones ya superadas y que el paciente ya no tenga infección por SARS-CoV-2 en ese momento”, añade.
Disponibilidad de los tests rápidos
Hay que tener en cuenta que este virus era desconocido hasta hace unos meses. La secuencia de su genoma se publicó a mediados de enero (un tiempo muy corto dado que hacía muy poco que se había descubierto). Una vez que se conoce la secuencia de un genoma es relativamente rápido desarrollar una técnica de PCR. Sin embargo, para desarrollar pruebas rápidas que detecten antígenos o anticuerpos, el proceso es más lento.
Además, antes de comenzar a utilizar una determinada prueba de laboratorio, es necesario hacer una verificación de su capacidad diagnóstica. Para que una técnica de diagnóstico se pueda comercializar en el mercado europeo, es necesario que cumpla unos requisitos que garanticen su funcionamiento. Aun así, es imprescindible que cada centro diagnóstico compruebe que el test elegido funciona de acuerdo a las especificaciones que indica el fabricante y que certifican los diferentes organismos reguladores.
En el caso de las pruebas rápidas, que pueden realizarse fuera del laboratorio (por ejemplo, en una consulta médica), es importante que uno o varios centros de referencia se hagan responsables de esta verificación, para poder garantizar su buen funcionamiento una vez distribuidos.
¿Cómo realizar más pruebas?
Para incrementar la capacidad de realizar pruebas PCR es indispensable que se mantenga un buen suministro de reactivos y que estos puedan adaptarse a equipos automatizados con mayor capacidad de procesamiento de muestras por día. Por otra parte, si se puede llegar a disponer de pruebas rápidas fiables y sin problemas de suministro, se podrían utilizar como cribado para detectar a pacientes asintomáticos o bien a aquellos que ya han pasado la infección de forma leve sin haber tenido una confirmación mediante PCR. En resumen, la cuestión clave es la disponibilidad de suministro y la calidad del resultado. “La exigencia de calidad es ineludible ante la necesidad de obtener un diagnóstico”, destaca la Dra. Caballé.
Fuente: SEQC-ML