Normalmente, tarda unos de ocho años todo el proceso que debe seguir un fármaco a través de ensayos clínicos para finalmente ser aprobado por la de Estados Unidos.
En la pandemia actual, los pacientes no tienen este tiempo para esperar las terapias para la COVID-19. ¿Cómo se puede acelerar de manera responsable la innovación, el acceso a los medicamentos experimentales y las aprobaciones de la FDA durante esta emergencia de salud pública?
No faltan las llamadas para actuar más rápidamente en respuesta a esta pandemia. Mike Ryan, el director ejecutivo del programa de emergencias sanitarias de la Organización Mundial de la Salud (OMS), por ejemplo, instó a todos en una conferencia de prensa esta semana: “Sean rápidos. No tengan remordimientos… El virus terminará alcanzándolos si no se mueven rápidamente… Si necesitan estar seguros antes de hacer sus movimientos, nunca ganarán… Todos tienen miedo a las consecuencias del error. Pero el mayor error es no hacer nada. El mayor error es sentirse paralizado por el miedo al fracaso”.
Dejando a un lado la ética de actuar sin la debida precaución o sin datos, vale la pena señalar que Estados Unidos ha estado acelerando el proceso de aprobación de medicamentos y aprobando drogas con menos evidencia durante años. Las revisiones de medicamentos de la FDA ahora toman menos de un año, y solo 53% de los medicamentos son aprobados con base en al menos dos ensayos claves, en contraste con el 81% en el pasado. Tampoco es raro ver un medicamento aprobado en gran parte en función de los datos de la Fase 2, sin un ensayo de Fase 3 completo, particularmente en oncología.
Aun así, esta aceleración no es suficiente en esta pandemia. La realización de ensayos clínicos suele ser la mejor manera de avanzar en el desarrollo de medicamentos y poner a disposición de los pacientes medicamentos experimentales, pero sus cronogramas y los estrictos criterios de inclusión dejan a muchos pacientes sin acceso a medicamentos durante muchos años.
La siguiente mejor opción puede ser ampliar los programas de acceso, diseñados para proporcionar medicamentos experimentales a pacientes con afecciones graves que no pueden inscribirse en un ensayo. Permiten la seguridad de los medicamentos y la recopilación de datos de eficacia, con el objetivo de apoyar tanto el desarrollo como el acceso a los medicamentos. En última instancia, el fabricante de cada medicamento debe aceptar proporcionar acceso a los medicamentos y tener un suministro suficiente para satisfacer las solicitudes. La pregunta es: ¿cuál es la probabilidad de que los programas de acceso ampliado puedan funcionar frente a esta pandemia?
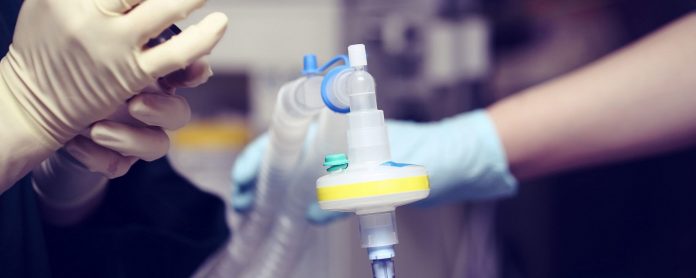
Un ejemplo es el remdesivir de Gilead, un prometedor medicamento para la COVID-19, según la OMS. Además de los niños gravemente enfermos, las mujeres embarazadas y los trabajadores del Departamento de Defensa, los pacientes que buscan acceder al remdesivir para tratar la COVID-19 deben inscribirse en un ensayo clínico o en el programa de acceso ampliado de Gilead. Este programa es para pacientes con COVID-19 que están hospitalizados y requieren ventilación mecánica. Por lo general, los médicos también pueden solicitar un acceso ampliado a medicamentos experimentales para pacientes individuales fuera de los programas grupales. Sin embargo, Gilead suspendió las solicitudes individuales a fines de marzo.
La ética de suspender las solicitudes de acceso ampliado individuales es un desafío. En el lado positivo, los programas grupales ahorran tiempo. Las solicitudes individuales requieren revisiones que requieren mucho tiempo de diversas partes, una perspectiva agotadora cuando miles de solicitudes inundan un sistema en un corto período de tiempo durante una pandemia. Sin embargo, existe la posibilidad de que los médicos intuben a los pacientes con COVID-19 antes de lo normal para que califiquen para el programa de acceso ampliado. Existe evidencia anecdótica de que esto sucede. En estos casos, es probable que los médicos determinen que los riesgos de la intubación temprana se compensan con los beneficios potenciales de obtener acceso a remdesivir, a pesar de la falta de los datos finales de ensayos clínicos. Entonces, el acceso puede convertirse en una función de qué tan dispuesto está un médico a trabajar con un sistema de acceso expandido para su paciente, produciendo un sistema inherentemente desigual.
En eventos masivos de cuidados críticos, como la pandemia actual, la bioética generalmente da paso a la ética de la salud pública. Mientras que la bioética se enfoca tradicionalmente en la salud y los intereses de los pacientes individuales y la interacción privada médico-paciente, la ética de la salud pública se enfoca en grupos y decisiones de las autoridades responsables de un gran número de personas. La bioética tiende a guiarse por principios como el respeto a la autonomía del individuo, mientras que la ética de la salud pública se basa en la justicia social y la distribución justa de los recursos sociales.
Este cambio en la orientación ética se considera crítico para salvar la mayor cantidad posible de vidas. En el triaje pandémico, por ejemplo, generalmente se prioriza a los más necesitados y más propensos a beneficiarse. Además, se analiza quién se beneficiará más rápido, con menos recursos. Si se pueden salvar dos personas en el tiempo que llevaría salvar una, la opción es clara. Estas no son buenas noticias para el paciente único.
Hoy, los médicos que están en la primera línea de esta pandemia enfrentan problemas desafiantes. ¿Deberían permanecer centrados en el paciente, trabajando en función de los sistemas para que sus pacientes con COVID-19 tengan acceso a medicamentos y otras intervenciones experimentales? Si es así, no están pensando necesariamente en otros pacientes o en el panorama general, sino que están pensando en la salud del paciente que tienen justo frente a ellos. En este escenario, un médico sigue siendo un defensor del paciente, mientras que una empresa, como Gilead, se centra en los resultados en la salud de la población. Esto puede no maximizar las vidas salvadas y exacerbar las desigualdades. Y bien podría influir en las decisiones de los médicos, como intubar antes para dar a sus pacientes acceso a un tratamiento experimental. Pero también puede proteger a los médicos del sentimiento de haber abandonado a sus pacientes. Estas son decisiones difíciles. Los comités de ética de los hospitales y los Centros para el Control y la Prevención de Enfermedades (CDC) de Estados Unidos deben proporcionar pautas –lo ideal sería con la participación de todas las partes interesadas, incluidos los pacientes– para ayudar a tomar estas decisiones éticas.
La FDA está trabajando en estrecha colaboración con los innovadores para acelerar sus esfuerzos, aprovechando la información científica sobre el virus y sobre los ensayos clínicos en curso en todo el mundo. Confiamos en que estos esfuerzos tendrán un efecto positivo importante en esta pandemia.1
Autores: John D. Loike y Jennifer E. Miller2
Fuente: REC
Referencias
- Puede consultar el artículo completo, en inglés, haciendo clic aquí.
- John D. Loike es profesor de biología en Touro College and University Systems. Jennifer E. Miller es profesora asistente en la Escuela de Medicina de Yale y es la fundadora de Bioethics International y Good Pharma Scorecard.