Palabras de la Dra. Graciela Borthagaray


 Más información: colabiocli2017uy.com
Más información: colabiocli2017uy.com
#colabiocli17 Acto Inagural del XXIII Congreso Latinoamericano de Química Clínica
Listado de emisiones anteriores
- Radio el Microscopio Segunda Década Emisión 626
- Radio el Microscopio Segunda Década Emisión 625
- Radio el Microscopio Segunda Década Emisión 624
- Radio el Microscopio Segunda Década Emisión 623
- Radio el Microscopio Segunda Década Emisión 622
- Radio el Microscopio Segunda Década Emisión 621
- Radio el Microscopio Segunda Década Emisión 620
- Radio el Microscopio Segunda Década Emisión 618
- Radio el Microscopio Segunda Década Emisión 617
- Radio el Microscopio Segunda Década Emisión 616
- Radio el Microscopio Segunda Década Emisión 615
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 600
- Radio el Microscopio Segunda Década Emisión 614
- Radio el Microscopio Segunda Década Emisión 613
- Radio el Microscopio Segunda Década Emisión 612
- Radio el Microscopio Segunda Década Emisión 611
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 610
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 609
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 608
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 607
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 606
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 605
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 604
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 602
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 601
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 599
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 598
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 597
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 596
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 595
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 594
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 593
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 592
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 591
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 590
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 589
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 588
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 587
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 586
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 585
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 584
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 583
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 582
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 581
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 580
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 578
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 577
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 576
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 573
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 572
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 571
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 570
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 569
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 568
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 567
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 566
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 565
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 564
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 563
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 562
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 561
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 560
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 559
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 558
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 557
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 556
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 555
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 554
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 553
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 552
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 551
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 550
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 549
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 548
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 547
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 546
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 545
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 544
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 543
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 542
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 541
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 540
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 539
- Radio el Microscopio Segunda Década – Formato Podcast Emisión 538
- Radio el Microscopio Segunda Década – Formato Podcast. Emisión 536
- Radio el Microscopio Segunda Década – Formato Podcast. Emisión 535
- Radio el Microscopio Segunda Década – Formato Podcast. Emisión 534
- Radio el Microscopio Segunda Década – Formato Podcast. Emisión 533
- Radio el Microscopio Segunda Década – Formato Podcast. Emisión 532
- Radio el Microscopio Segunda Década – Formato Podcast. Emisión 531
- Radio el Microscopio Segunda Década – Formato Podcast. Emisión 527
- El Microscopio. Radio Bioquímica on line. Emisión 509.
- El Microscopio. Radio Bioquímica on line. Emisión 494.
- El Microscopio. Radio on line bioquímica. Emisión 489.
- El Microscopio. Radio on line Bioquímica. Emisión 487.
- El Microscopio. Radio on line Bioquímica. Emisión 486
- El Microscopio, radio online bioquímica – Emisión 459
- El Microscopio, radio online bioquímica – Emisión 448
- El Microscopio – Emisión 442
- El Microscopio – Emisión 441
- El Microscopio – Emisión 440
- El Microscopio – Emisión 439
- El Microscopio – Emisión 438
- El Microscopio – Emisión Especial año nuevo
- El Microscopio – Emisión Especial Navidad
- El Microscopio – Emisión 436
- El Microscopio – Emisión 432
- El Microscopio – Emisión 431
- El Microscopio – Emisión 430
- El Microscopio – Emisión 428
- El Microscopio – Emisión 427
- El Microscopio – Emisión 426
- El Microscopio – Emisión 416
- El Microscopio – Emisión 414
- Entrevista con el Dr. Khosrow Adeli, presidente de la IFCC
- El Microscopio – Emisión 409
- El Microscopio – Emisión 408
- El Microscopio – Emisión 407
- El Microscopio – Emisión 399
- El Microscopio – Emisión 398
- El Microscopio – Emisión 397
- El Microscopio – Emisión 395
- El Microscopio – Emisión 391
- El Microscopio – Emisión 390
- El Microscopio – Emisión 389
- El Microscopio – Emisión 388
- El Microscopio – Emisión 387
- El Microscopio – Emisión 384
- El Microscopio – Emisión 383
- El Microscopio – Emisión 382
- El Microscopio – Emisión 381
- El Microscopio – Emisión 378
- El Microscopio – Emisión 377
- El Microscopio – Emisión 376
- El Microscopio – Emisión 375
- El Microscopio – Emisión 374
- El Microscopio – Emisión 373
- Congresos y Cursos bajo auspicio de la IFCC – Julio 2019
- El Microscopio – Emisión 372
- El Microscopio – Emisión 370
- El Microscopio – Emisión 369
- El Microscopio – Emisión 368
- El Microscopio – Emisión 367
- El Microscopio – Emisión 364
- El Microscopio – Emisión 363
- El Microscopio – Emisión 362
- El Microscopio – Emisión 360
- El Microscopio – Emisión 359
- El Microscopio – Emisión 357
- El Microscopio – Emisión 356
- El Microscopio – Emisión 355
- El Microscopio – Emisión 354
- El Microscopio – Emisión 353
- El Microscopio – Emisión 352
- El Microscopio – Emisión 350
- El Microscopio – Emisión 349
- El Microscopio – Emisión 348
- El Microscopio – Emisión 347
- El Microscopio – Emisión 346
- El Microscopio – Emisión 344
- El Microscopio – Emisión 343
- El Microscopio – Emisión 342
- El Microscopio – Emisión 341
- El Microscopio – Emisión 340
- El Microscopio – Emisión 337
- El Microscopio – Emisión 336
- El Microscopio – Emisión 335
- El Microscopio – Emisión 334
- El Microscopio – Emisión 333
- El Microscopio – Emisión 332
- El Microscopio – Emisión 331
- El Microscopio – Emisión 330
- El Microscopio – Emisión 329
- El Microscopio – Emisión 328
- El Microscopio – Emisión 327
- El Microscopio – Emisión 326
- El Microscopio – Emisión 325
- El Microscopio – Emisión 324
- El Microscopio – Emisión 323
- El Microscopio – Emisión 322
- El Microscopio – Emisión 321
- El Microscopio – Emisión 320
- El Microscopio – Emisión 319
- El Microscopio – Emisión 318
- El Microscopio – Emisión 317
- El Microscopio – Emisión 316
- El Microscopio – Emisión 315
- El Microscopio – Emisión 314
- El Microscopio – Emisión 313
- El Microscopio – Emisión 311
- El Microscopio – Emisión 310
- El Microscopio – Emisión 309
- El Microscopio – Emisión 308
- El Microscopio – Emisión 307
- El Microscopio – Emisión 306
- El Microscopio – Emisión 305
- El Microscopio – Emisión 304
- El Microscopio – Emisión 303
- El Microscopio – Emisión 302
- El Microscopio – Emisión 301
- El Microscopio – Emisión 300
- El Microscopio – Emisión 299
- El Microscopio – Emisión 298
- El Microscopio – Emisión 297
- El Microscopio – Emisión 296
- El Microscopio – Emisión 295
- El Microscopio – Emisión 294
- El Microscopio – Emisión 293
- El Microscopio – Emisión 292
- El Microscopio – Emisión 291
- El Microscopio – Emisión 290
- El Microscopio – Emisión 289
- El Microscopio – Emisión 288
- El Microscopio – Emisión 287
- El Microscopio – Emisión 286
- El Microscopio – Emisión 285
- El Microscopio – Emisión 284
- Revista Diagnóstico in Vitro – DIV Octubre 2017
- El Microscopio – Emisión 283
- El Microscopio – Emisión 282
- El Microscopio – Emisión 281
- El Microscopio – Emisión 280
- El Microscopio – Emisión 279
- El Microscopio – Emisión 278
- El Microscopio – Emisión 277
- El Microscopio – Emisión 276
- El Microscopio – Emisión 275
- El Microscopio – Emisión 274
- El Microscopio – Emisión 273
- El Microscopio – Emisión 272
- El Microscopio – Emisión 271
- El Microscopio – Emisión 270
- El Microscopio – Emisión 269
- El Microscopio – Emisión 268
- El Microscopio – Emisión 267
- El Microscopio – Emisión 266
- El Microscopio – Emisión 265
- El Microscopio – Emisión 264
- El Microscopio – Emisión 263
- El Microscopio – Emisión 262
- El Microscopio – Emisión 261
- El Microscopio – Emisión 260
- El Microscopio – Emisión 259
- El Microscopio – Emisión 258
- El Microscopio – Emisión 257
- El Microscopio – Emisión 256
- El Microscopio – Emisión 255
- El Microscopio – Emisión 254
- El Microscopio – Emisión 253
- Entrevista con el Dr. Leverton Ortiz (Chile): Atención Bioquímica
- El Microscopio – Emisión 252
- El Microscopio – Emisión 251
- El Microscopio – Emisión 250
- El Microscopio – Emisión 248
- El Microscopio – Emisión 247
- El Microscopio – Emisión 246
- El Microscopio – Emisión 245
- El Microscopio – Emisión 244
- El Microscopio – Emisión 243
- El Microscopio – Emisión 242
- El Microscopio – Emisión 241
- El Microscopio – Emisión 240
- El Microscopio – Emisión 239
- Reporte Epidemiológico 239
- El Microscopio – Emisión 238
- El Microscopio – Emisión 236
- Reporte Epidemiológico 236
- El Microscopio – Emisión 235
- El Microscopio – Emisión 234
- Reporte Epidemiológico 234
- El Microscopio – Emisión 233
- El Microscopio – Emisión 232
- El Microscopio – Emisión 231
- El Microscopio – Emisión 230
- El Microscopio – Emisión 229
- Reporte Epidemiológico 229
- El Microscopio – Emisión 228
- El Microscopio – Emisión 227
- Resultados de la Elección del Presidente de la IFCC 2017-2020
- El Microscopio – Emisión 226
- El Microscopio – Emisión 225
- El Microscopio – Emisión 224
- El Microscopio – Emisión 223
- Definir la fertilidad en base a un análisis de semen es complicado
- El Microscopio – Emisión 222
- Reporte Epidemiológico 222
- El Microscopio – Emisión 221
- El Microscopio – Emisión 220
- El Microscopio – Emisión 218
- El Microscopio – Emisión 217
- Entrevista con el Dr. Álvaro Justiniano Grosz (Bolivia): Cursos PROBOECO
- El Microscopio – Emisión 216
- El Microscopio – Emisión 215
- El Microscopio – Emisión 214
- El Microscopio – Emisión 213
- El Microscopio – Emisión 212
- El Microscopio – Emisión 211
- El Microscopio – Emisión 210
- Reporte Epidemiológico 210
- El Microscopio – Emisión 208
- Nuevo Webinar de la IFCC sobre Acreditación del Laboratorio Médico
- El Microscopio – Emisión 207
- El Microscopio – Emisión 206
- El Microscopio – Emisión 205
- El Microscopio – Emisión 204
- El Microscopio – Emisión 203
- El Microscopio – Emisión 202
- Reporte Epidemiológico 199
- #IFCCGC2016 Grupo de Trabajo Iberoamericano de Traducciones y Nomenclatura en la cena de recepción de la AEFA
- El Microscopio – Emisión 197
- El Microscopio – Emisión 196
- Reporte Epidemiológico 196
- El Microscopio – Emisión 194
- El Microscopio – Emisión 193
- El Microscopio – Emisión 192
- El Microscopio – Emisión 189
- El Microscopio – Emisión 186
- El Microscopio – Emisión 185
- El Microscopio – Emisión 183
- El Microscopio – Emisión 181
- Reporte Epidemiológico 180
- El Microscopio – Emisión 180
- El Microscopio – Emisión 179
- Reporte Epidemiológico 179
- El Microscopio – Emisión 178
- Reporte Epidemiológico 177
- El Microscopio – Emisión 177
- El Microscopio – Emisión 176
- Reporte Epidemiológico 175
- El Microscopio – Emisión 175
- El Microscopio – Emisión 174
- El Microscopio – Emisión 173
- El Microscopio – Emisión 172
- El Microscopio – Emisión 171
- El Microscopio – Emisión 170
- El Microscopio – Emisión 169
- El Microscopio – Emisión 168
- El Microscopio – Emisión 167
- El Microscopio – Emisión 166
- El Microscopio – Emisión 165
- El Microscopio – Emisión 164
- El Microscopio – Emisión 163
- El Microscopio – Emisión 162
- Entrevista con el Dr. Álvaro Justiniano Grosz (Bolivia): 18° Congreso Nacional Ordinario de la Sociedad Boliviana de Bioquímica Clínica
- El Microscopio – Emisión 160
- Reporte Epidemiológico 154
- El Microscopio – Emisión 154
- Entrevista con el Dr. Álvaro Justiniano Grosz (Bolivia): XVIII Congreso Nacional Ordinario de la Sociedad Boliviana de Bioquímica Clínica
- El Microscopio – Emisión 153
- El Microscopio – Emisión 152
- El Microscopio – Emisión 151
- El Microscopio – Emisión 150
- El Microscopio – Emisión 147
- El Microscopio – Emisión 144
- El Microscopio – Emisión 143
- El Microscopio – Emisión 142
- El Microscopio – Emisión 141
- Entrevista con la Dra. Isabel Fierro (Ecuador): Gestión en la Universidad Central del Ecuador
- El Microscopio – Emisión 140
- Entrevista con el Dr. Leverton Ortiz (Chile): Point of Care Testing y su evolución
- El Microscopio – Emisión 139
- El Microscopio – Emisión 138
- El Microscopio – Emisión 137
- El Microscopio – Emisión 136
- El Microscopio – Emisión 135
- El Microscopio – Emisión 134
- Editorial: mensaje del Presidente de la IFCC, el Dr. Graham Beastall
- El Microscopio – Emisión 133
- El Microscopio – Emisión 132
- El Microscopio – Emisión 131
- El Microscopio – Emisión 130
- El Microscopio – Emisión 129
- El Microscopio – Emisión 128
- El Microscopio – Emisión 127
- El Microscopio – Emisión 126
- El Microscopio – Emisión 125
- El Microscopio – Emisión 124
- El Microscopio – Emisión 123
- El Microscopio – Emisión 122
- El Microscopio – Emisión 121
- El Microscopio – Emisión 120
- El Microscopio – Emisión 119
- Entrevista con la Dra. María del Carmen Pasquel (Ecuador): Importancia de asistir a Congresos Internacionales
- El Microscopio – Emisión 118
- El Microscopio – Emisión 117
- El Microscopio – Emisión 116
- El Microscopio – Emisión 115
- El Microscopio – Emisión 114
- El Microscopio – Emisión 113
- El Microscopio – Emisión 111
- Entrevista con el Prof. Howard Morris (Australia): Armonización y estandarización en los laboratorios
- El Microscopio – Emisión 109
- El Microscopio – Emisión 108
- El Microscopio – Emisión 106
- El Microscopio – Emisión 107
- El Microscopio – Emisión 105
- El Microscopio – Emisión 104
- El Microscopio – Emisión 103
- El Microscopio – Emisión 102
- El Microscopio – Emisión 101
- El Microscopio – Emisión 100
- El Microscopio – Emisión 99
- El Microscopio – Emisión 98
- El Microscopio – Emisión 97
- El Microscopio – Emisión 96
- El Microscopio – Emisión 95
- El Microscopio – Emisión 94
- El Microscopio – Emisión 93
- El Microscopio – Emisión 92
- El Microscopio – Emisión 91
- El Microscopio – Emisión 90
- El Microscopio – Emisión 89
- El Microscopio – Emisión 88
- El Microscopio – Emisión 87
- El Microscopio – Emisión 86
- El Microscopio – Emisión 85
- El Microscopio – Emisión 84
- El Microscopio – Emisión 83
- El Microscopio – Emisión 82
- El Microscopio – Emisión 81
- El Microscopio – Emisión 80
- El Microscopio – Emisión 79
- El Microscopio – Emisión 78
- El Microscopio – Emisión 76
- El Microscopio – Emisión 75
- El Microscopio – Emisión 74
- El Microscopio – Emisión 72
- El Microscopio – Emisión 71
- El Microscopio – Emisión 70
- El Microscopio – Emisión 69
- El Microscopio – Emisión 68
- El Microscopio – Emisión 67
- Entrevista con el Dr. Christian Jaroszewsky (Argentina): Desafíos en la Bioquímica Forense
- El Microscopio – Emisión 66
- El Microscopio – Emisión 65
- El Microscopio – Emisión 64
- El Microscopio – Emisión 63
- El Microscopio – Emisión 61
- El Microscopio – Emisión 60
- El Microscopio – Emisión 59
- El Microscopio – Emisión 58
- El Microscopio – Emisión 57
- El Microscopio – Emisión 56
- El Microscopio – Emisión 55
- El Microscopio – Emisión 54 – Aniversario
- El Microscopio – Emisión 53
- El Microscopio – Emisión 52
- El Microscopio – Emisión 51
- Entrevista con el Dr. Oswaldo Ruiz Narváez (Costa Rica)
- El Microscopio – Emisión 50
- El Microscopio – Emisión 49
- El Microscopio – Emisión 48
- El Microscopio – Emisión 47 – Especial Jóvenes Bioquímicos
- El Microscopio – Emisión 45
- El Microscopio – Emisión 44
- El Microscopio – Emisión 43
- El Microscopio – Emisión 41
- El Microscopio – Emisión 40 – Especial Kuala Lumpur
- El Microscopio – Emisión 39 – Especial Premio Nobel
- El Microscopio – Emisión 38
- El Microscopio – Emisión 37
- El Microscopio – Emisión 36
- El Microscopio – Emisión 35
- El Microscopio – Emisión 33
- El Microscopio – Emisión 32
- El Microscopio – Emisión 31
- El Microscopio – Emisión 30
- El Microscopio – Emisión 29
- El Microscopio – Emisión 28
- El Microscopio – Emisión 27
- El Microscopio – Emisión 26
- El Microscopio – Emisión 25
- El Microscopio – Emisión 24
- El Microscopio – Emisión 23
- El Microscopio – Emisión 22
- Entrevista con la Dra. Miriam Aguilera (Honduras)
- El Microscopio – Emisión 21
- El Microscopio – Emisión 20
- El Microscopio – Emisión 19
- El Microscopio – Emisión 17
- El Microscopio – Emisión 16
- El Microscopio – Emisión 15
- El Microscopio – Emisión 14
- Entrevista con la Dra. María del Carmen Pasquel (Ecuador): Calidad en el Laboratorio, debate múltiple
- El Microscopio – Emisión 13
- El Microscopio – Emisión 12
- El Microscopio – Emisión 11
- El Microscopio – Emisión 10
- El Microscopio – Emisión 09
- El Microscopio – Emisión 08
- El Microscopio – Emisión 06
- El Microscopio – Emisión 05
- El Microscopio – Emisión 04
- El Microscopio – Emisión 03
- El Microscopio – Emisión 02
- El Microscopio – Emisión 01
#colabiocli17 ¡Hoy comienza el XXIII Congreso Latinoamericano de Química Clínica!
Esta reunión permite informar y discutir sobre avances científicos y tecnológicos en el área de laboratorio clínico, encontrar especialistas de renombre internacional, intercambiar experiencias y oportunidades de colaboración, y principalmente reencontrar colegas y amigos.
El programa de actividades incluye, conferencias magistrales, simposios, cursos de actualización, presentaciones de temas libres, que abarcan temas de bioquímica, pesquisa neonatal, microbiología, hematología, inmunología, parasitología, nuevas aplicaciones de citometría de flujo, HPLC y biología molecular, farmacogenética, así bioética, gestión de calidad y gerenciamiento y acreditación de carreras en el ámbito latinoamericano.
Una experiencia de enriquecimiento científico y cultural, que por primera vez se desarrolla en Uruguay.
Página web del Congreso: colabiocli2017uy.com
Entrevistas realizadas en El Microscopio:
- Entrevista con la Dra. Rosa Sierra Amor sobre el Taller Verificación de Métodos Analíticos en COLABIOCLI 2017
- Entrevista con la Dra. Patricia Esperón (Uruguay): Eje de genética en COLABIOCLI 2017
- Entrevista con la Dra. Cristina Servetto (Uruguay): Eje de Química Clínica en COLABIOCLI 2017.
- Entrevista con la Dra. Stella Raymondo (Uruguay): Eje de Calidad en COLABIOCLI 2017
- Entrevista con la Dra. Carolina Márquez (Uruguay): Eje de Microbiología en COLABIOCLI 2017
- Entrevista con la Dra. Ana Lena (Uruguay): Hematología y Hemostasia en COLABIOCLI 2017
- Entrevista con la Dra. Graciela Borthagaray (Uruguay): COLABIOCLI 2017
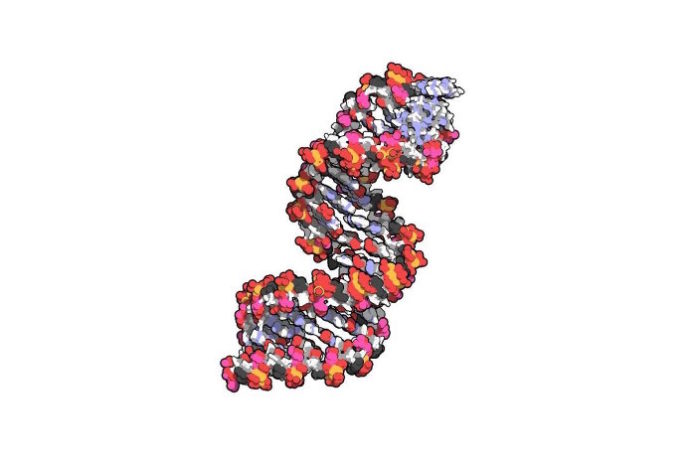
miR-323-3p circulante es un biomarcador de cardiomiopatía y un indicador de variabilidad fenotípica en pacientes de ataxia de Friedreich
A pesar de este último hecho, se considera una enfermedad rara o poco frecuente con un debut en la infancia y presenta una progresiva pérdida de las neuronas sensitivas en el ganglio dorsal de la raíz y la columna posterior de la médula. Además de presentar alteraciones en el sistema nervioso periférico (Harding, 1981; Pandolfo, 2009), el sistema nervioso central también está afectado, detectando alteraciones en el núcleo dentado del cerebelo de estos pacientes (Koeppen, 2011). Al mismo tiempo de estas características neurológicas, otras enfermedades concomitantes se han descrito en pacientes de FRDA. Así, los pacientes de FRDA pueden presentar, además de mostrar las características neurológicas, escoliosis, diabetes tipo II y cardiomiopatía hipertrófica (Durr, 1996; Delatycki, 1999). Esta última es la principal causa de muerte en pacientes de FRDA. El fenotipo observado en pacientes de FRDA está causado por una alteración en el número de repeticiones del tripéptido guanina-adenina-adenina (GAA) en el primer intrón del gen FXN que codifica para la proteína frataxina. En el caso de la ataxia de Friedreich las repeticiones fluctúan entre 44 y 1700 y generan la disminución de expresión de la proteína frataxina (Pandolfo, 2009; Sharma, 2004). La función principal de frataxina no está claramente corroborada, sin embargo, esta proteína se ha visto implicada en diversas funciones como la de almacenaje de hierro o la formación de los clústeres hierro-azufre (Puccio, 2001; Rotig, 1997). Este tipo de ataxia, presenta diferencias en las características clínicas, así como en la progresión de la enfermedad. Además, la presencia de enfermedades concomitantes incrementa la complejidad de esta neuropatía, por lo que se está incrementando el estudio de posibles biomarcadores pronóstico de esta enfermedad. No obstante, no existen biomarcadores fiables que puedan estratificar los pacientes según su enfermedad/es concomitante/s (diabetes, escoliosis y cardiomiopatía hipertrófica).
Los microARNs (miARN) son pequeñas secuencias de 22 nucleótidos localizadas en regiones intragénicas y/o intrínsecas de transcritos que codifican para proteínas. Tras su procesamiento por el complejo Drosha-DGCR8 (Gregory, 2004) y Dicer (Chantrel-Groussard, 2001), dos hebras complementarias se generan y una es incorporada al complejo de silenciamiento inducido de ARN (Bartel, 2004). Este complejo se une por complementariedad a la secuencia de ARN mensajero de la proteína diana controlando su degradación, y por tanto los niveles de proteína. Estas pequeñas moléculas genómicas han sido descritas como biomarcadores de diferentes enfermedades y ha sido descrita su implicación en el desarrollo y correcto funcionamiento del sistema nervioso (Fiore, 2011). Por ello, el estudio de los perfiles de expresión de estos miARN puede proporcionar más conocimiento acerca de los mecanismos patológicos de las enfermedades neurodegenerativas además de servir como biomarcadores de progresión de la enfermedad y monitorización de los tratamientos que se utilicen durante los ensayos clínicos.
En el análisis del miRNoma de las muestras de plasma encontramos siete miARN circulantes que tienen expresión diferencial entre pacientes de ataxia de Friedreich y sujetos control (hsa-miR-128-3p, hsa-miR-625-3p, hsa-miR-130b-5p, hsa-miR-151a-5p, hsa-miR-330-3p, hsa-miR-323a-3p, hsa-miR-142-3p). Además, al realizar análisis para estratificar los pacientes encontramos que el mir-323a-3p presenta niveles más elevados en aquellos pacientes con cardiomiopatía hipertrófica con una alta sensibilidad (88.9%) y una aceptable especificidad (62.5%). Este miARN puede ayudar a los clínicos en la generación de algoritmos que predigan la cardiomiopatía en este tipo de enfermos, contribuyendo a un diagnóstico y pronóstico temprano previo a la detección por procedimientos estándar.
Referencia: Seco-Cervera, M. et al. Circulating miR-323-3p is a biomarker for cardiomyopathy and an indicator of phenotypic variability in Friedreich’s ataxia patients. Sci Rep. 2017 Jul 12;7(1):5237. doi: 10.1038/s41598-017-04996-9.
Biografía:
- Bartel DP. MicroRNAs: genomics, biogenesis, mechanism, and function. Cell. 2004 Jan 23;116(2):281-97.
- Chantrel-Groussard K, et al. Disabled early recruitment of antioxidant defenses in Friedreich’s ataxia. Hum Mol Genet. 2001 Sep 15;10(19):2061-7.
- Delatycki MB, et al. Clinical and genetic study of Friedreich ataxia in an Australian population. Am J Med Genet. 1999 Nov 19;87(2):168-74.
- Dürr A, et al. Clinical and genetic abnormalities in patients with Friedreich’s ataxia. N Engl J Med. 1996 Oct 17;335(16):1169-75.
- Fiore R, et al. MicroRNA function in the nervous system. Prog Mol Biol Transl Sci. 2011;102:47-100. doi: 10.1016/B978-0-12-415795-8.00004-0
- Gregory RI, et al. The Microprocessor complex mediates the genesis of microRNAs. Nature. 2004 Nov 11;432(7014):235-40.
- Harding AE. Friedreich’s ataxia: a clinical and genetic study of 90 families with an analysis of early diagnostic criteria and intrafamilial clustering of clinical features. Brain. 1981 Sep;104(3):589-620.
- Koeppen AH. Friedreich’s ataxia: pathology, pathogenesis, and molecular genetics. J Neurol Sci. 2011 Apr 15;303(1-2):1-12.doi: 10.1016/j.jns.2011.01.010
- Pandolfo M. Friedreich ataxia: the clinical picture. J Neurol. 2009 Mar;256 Suppl 1:3-8.doi: 10.1007/s00415-009-1002-3.
- Puccio H, et al. Mouse models for Friedreich ataxia exhibit cardiomyopathy, sensory nerve defect and Fe-S enzyme deficiency followed by intramitochondrial iron deposits. Nat Genet. 2001 Feb;27(2):181-6
- Rötig A, et al. Aconitase and mitochondrial iron-sulphur protein deficiency in Friedreich ataxia. Nat Genet. 1997 Oct;17(2):215-7.
- Sharma R, et al. Friedreich ataxia in carriers of unstable borderline GAA triplet-repeat alleles. Ann Neurol. 2004 Dec;56(6):898-901.
Fuente: Revista Genética Médica
Sepsis-3 y las nuevas definiciones, ¿es tiempo de abandonar SIRS?
Recientemente, el Grupo de Trabajo de las Definiciones de Sepsis (Sepsis Definitions Task Force) ha publicado un consenso con las definiciones actualizadas de sepsis y shock séptico (SEPSIS-3) que utiliza un nuevo concepto de sepsis como disfunción orgánica potencialmente mortal causada por una respuesta disregulada del huésped a la infección, utilizando el sistema de puntuación SOFA (Sequential Organ Failure Assessment), y propugna se abandonen los antiguos criterios. Realizamos una revisión de los antecedentes de esta nueva propuesta de definición, las definiciones planteadas por este nuevo consenso, comparando estas nuevas definiciones con las antiguas, limitaciones y evaluamos su aplicabilidad en la práctica clínica.
El término sepsis fue introducido por Hipócrates en el siglo IV a.C. como un proceso por el cual la carne se descompone y las heridas se infectan. Sin embargo, ante la inexistencia de una definición o criterios diagnósticos uniformes, en 1992 se publicó el consenso del American College of Chest Physicians y la Society of Critical Care Medicine Consensus Conference para uniformizar los criterios diagnósticos y lograr la oportuna “sospecha diagnóstica”, criterios que provocaron controversia desde el momento en que fueron presentados.
En los últimos años, los avances en los conocimientos de la fisiopatología, han demostrado que las infecciones provocan una respuesta compleja y variable del huésped, con mecanismos proinflamatorios y antiinflamatorios que pueden contribuir por un lado a la eliminación de la infección y la recuperación de los tejidos y por otro lado a la injuria de los órganos e infecciones secundarias; la respuesta va a depender del patógeno causal (carga y virulencia) y de las características genéticas y enfermedades coexistentes del huésped.
Descargue el PDF completo haciendo click aquí.
Autores: Elsa R Neira-Sanchez1,2,3, Germán Málaga1,3
- Departamento de Medicina, Hospital Nacional Cayetano Heredia. Lima, Perú.
- Universidad Peruana Cayetano Heredia. Lima, Perú.
- Conocimiento y Evidencia CONEVID, Universidad Peruana Cayetano Heredia. Lima, Perú
Citar: Neira-Sanchez ER, Málaga G. Sepsis-3 y las nuevas definiciones, ¿es tiempo de abandonar SIRS? Acta Med Peru. 2016;33(3):217-22.
X Simposio Internacional en Resistencia a los Antimicrobianos
Del 7 al 9 de Marzo de 2018, Universidad del Bosque, Santiago de Cali, Colombia.
Acceda al Programa Preliminar haciendo click aquí.
| Infobioquimica.org no dispone más datos que los aquí publicados. Por favor, si necesita más información envíe una consulta directa a los organizadores del evento. |
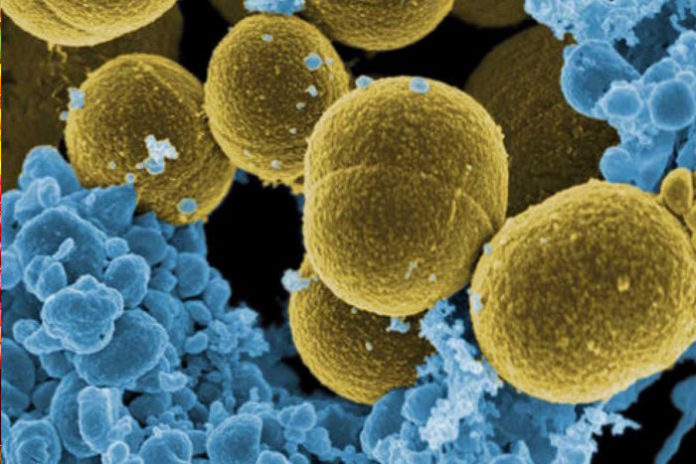
La importación ilegal de alimentos ayuda a propagar Staphylococcus aureus
Una investigación liderada por la Universidad de Burgos (UBU) ha descrito, por primera vez, microorganismos de relevancia en salud pública por su peligrosidad en alimentos decomisados en vuelos internacionales en distintos aeropuertos europeos. Este trabajo, enmarcado en un proyecto internacional financiado por la Unión Europea, se ha centrado en la caracterización de la presencia de cepas de Staphylococcus aureus multirresistentes a antibióticos.
Los resultados, publicados en la revista Frontiers in Microbiology, indican que el 26% de las casi mil muestras de alimentos analizadas fueron positivas para esta problemática bacteria. En el trabajo han participado investigadores de las universidades de Burgos y Valladolid, junto con profesionales del Instituto Tecnológico Agrario de Castilla y León (ITACyL), de los Hospitales Universitarios Río Hortega de Valladolid y de León, de la Delegación del Gobierno en el País Vasco y de la Universidad Veterinaria de Viena (Austria).
Como explica el profesor de la UBU David Rodríguez Lázaro, coordinador del estudio, Staphylococcus aureus ha sido seleccionado por la Organización Mundial de la Salud (OMS) el pasado mes de febrero como uno de los patógenos más relevantes para la salud pública.
Este tipo de microorganismos, y en particular las cepas resistentes a la meticilina (MRSA, del inglés Methicillin-resistant S. aureus), son una de las principales causas de infecciones en los hospitales en los países occidentales, y han sido encontradas en alimentos que transportaban pasajeros de vuelos internacionales en los aeropuertos de Bilbao y de Viena.
Por ello, el objetivo de este trabajo fue evaluar el papel potencial de la entrada ilegal de alimentos en la UE en la propagación de MRSA. Se estudió la prevalencia y las características de las cepas de MRSA aisladas de los alimentos de origen animal confiscados a los pasajeros en vuelos de 45 países no comunitarios de 2012 a 2015 por las Autoridades Fronterizas de los aeropuertos español y austriaco.
De las 868 muestras de alimentos analizadas (diversas de carne que incluyen antílope, pato, cobaya, cerdo, roedores, pavo, productos lácteos y huevos), 26 (el 3%) fueron positivas para MRSA. La prevalencia de muestras positivas entre los alimentos confiscados en el Aeropuerto Internacional de Bilbao fue del 11’8%. Más del 69% de los aislados de MRSA eran resistentes a tres o más tipos de agentes antimicrobianos.
“Este hallazgo revela tanto la gran diversidad de la resistencia antimicrobiana encontrada en las cepas como la capacidad de resistencia no solo a los fármacos beta-lactámicos. Por tanto, este estudio demuestra la presencia de MRSA en los alimentos que entran ilegalmente en la UE, y destaca la importación ilegal de alimentos como vía de su posible propagación”, detalla Rodríguez.
Prevenir infecciones en humanos
El trabajo pone de manifiesto la validez de la estrategia ‘una salud’, en la cual “todos los actores implicados en la Salud Pública (médicos, veterinarios, y microbiólogos de los alimentos) actúan de una forma coordinada planteando una acción integral para garantizar de una manera global la salud”, apunta el investigador principal, quien subraya que de esta manera “se puede garantizar que aspectos como la sanidad ambiental, la sanidad animal y la sanidad humana no estén disociados, y compartimentalizados de una manera rígida y sin conexión efectiva”.
En este sentido, continúa Rodríguez, “más del 60% de las infecciones humanas tienen carácter zoonótico, es decir, provienen de los animales y, por tanto, los alimentos que se obtienen de ellos pueden ser una fuente de contaminación muy apreciable”. Es por ello, concluye, “que el estudio de los mismos puede ser muy relevante para prevenir infecciones en humanos, y en particular con cepas bacterianas multirresistentes a antibióticos”.
Referencia bibliográfica: Rodriguez-Lazaro, D., Oniciuc, E. A., Gonzalez-Garcia, P., Gallego, D., Fernandez-Natal, I., Dominguez-Gil, M., … & Hernandez, M. (2017). “Detection and characterization of Staphylococcus aureus and Methicillin-resistant S. aureus in foods confiscated in EU borders”. Frontiers in Microbiology, 8, 1344
Fuente: Agencia Sinc
1º Taller de Actualización Científica del Grupo Franco-argentino de Investigación en Inmunología (Grupo FAIR): Inmunomodulación e Inmunoterapia
La Facultad de Ciencias Químicas (UNC), a través de su Departamento de Bioquímica Clínica y el Consejo Asesor de Actualización Profesional (CADAP), invita al 1º Taller de Actualización Científica del Grupo Franco-argentino de Investigación en Inmunología (Grupo FAIR): Inmunomodulación e Inmunoterapia (aprobado según Res. HCD 1013/17)
Esta actividad tendrá lugar el 23 de noviembre de 2017, de 8:30 a 18:30, en el Auditorio de la Facultad de Ciencias Químicas (UNC). “El taller está destinado a estudiantes de los últimos años de las carreras de Bioquímica y de otras carreras afines, estudiantes de posgrado y profesionales del área de la salud”, adelantó la Dra. Mariana Maccioni, directora del evento junto a la Dra. Eliane Piaggio, Directora de la Unidad de Inmunoterapia Traslacional del Institut Curie, París.
Disertantes:
- Matías Ostrowski. INBIRS-CONICET, UBA, Buenos Aires.
- Guillermo Docena. CONICET, ULP, La Plata.
- Eva Acosta Rodríguez. CIBICI-CONICET, UNC, Córdoba.
- Roxana Schillaci. Laboratorio de Mecánica Molecular de carcinogénesis, IBYME CONICET, Buenos Aires.
- Mariana Maccioni. CIBICI-CONICET, UNC, Córdoba.
- Juan Sabaté. Instituto de Investigaciones Médicas en Retrovirus y SIDA (INBIRS), Buenos Aires.
- Liliana Bezrodnik. Servicio Inmunología, Hospital de Niños “Ricardo Gutiérrez”; CONICET, Buenos Aires.
- Gabriel Morón. CIBICI-CONICET, UNC, Córdoba.
- Clotilde Thery. Institut Curie, París.
- Rachel Golub. Institut Pasteur, París.
- Philippe Benaroch. Institut Curie, París.
- Sebastian Amigorena. Institut Curie, París.
- Frederic Rieux-Laucat. Institut Imagine, Université París Descartes.
Acceda desde aquí al Programa del Taller.
Inscripciones
El 1º Taller del Grupo FAIR “Inmunomodulación e Inmunoterapia” no tendrá costo y abordará los últimos avances en la inmunología de temas tan relevantes para la salud como inmunodeficiencias, SIDA, cáncer, alergia e infecciones. Los interesados en solicitar certificado de asistencia deberán abonar 150 pesos. Las inscripciones serán recibidas hasta el 3 de noviembre de 2017 a través de un formulario electrónico.
Información y consultas:
| Infobioquimica.org no dispone más datos que los aquí publicados. Por favor, si necesita más información envíe una consulta directa a los organizadores del evento. |